-
蒸気の基本
-
蒸気の特性
-
-
-
水の状態図
図 1.1 は、先の「水の相」で述べた内容をグラフで表した、大気圧下にお ける水の状態図(相図)です。横軸を比エンタルピー、縦軸を温度として、加 熱(比エンタルピーの増加)による温度と相の変化を示しています。(図中左 側部分の氷や氷と水の混合状態は、蒸気工学分野ではあまり対象とされない為、説明は割愛します。)
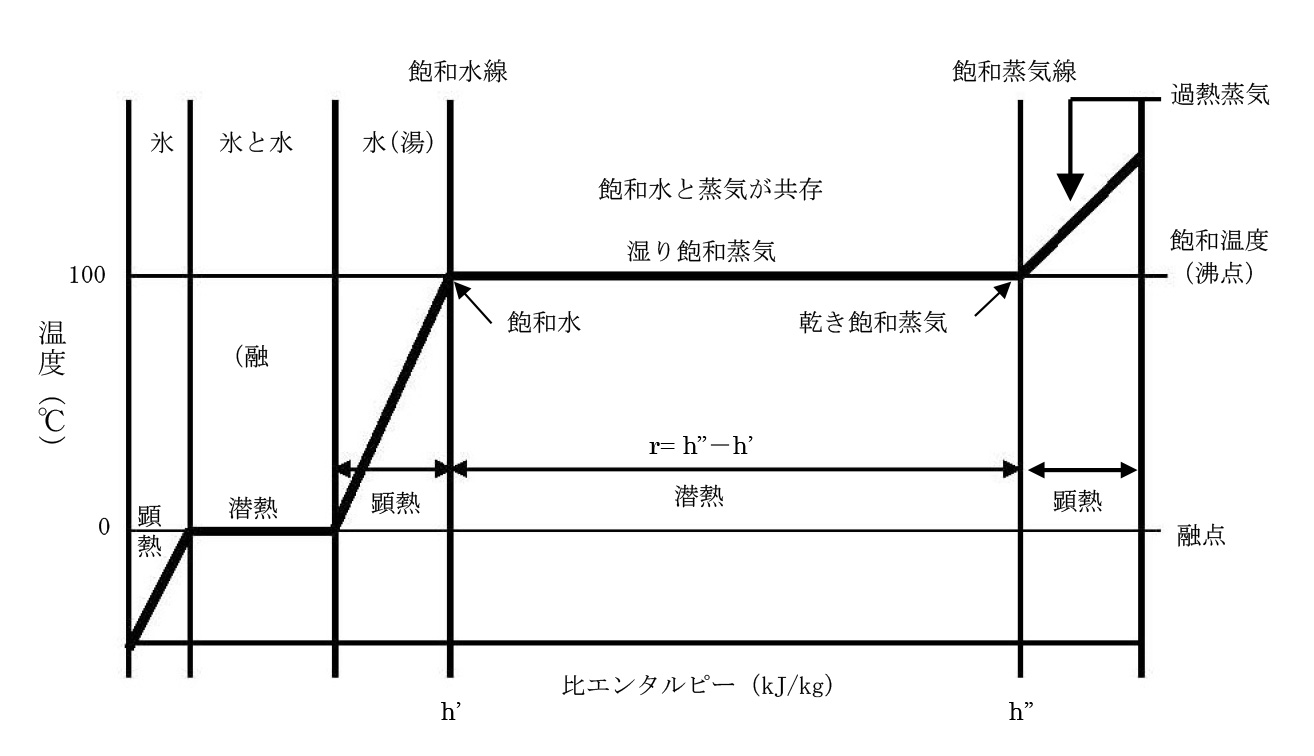
図 1.1 大気圧下における水の状態変化
温度 0℃から加熱し始めて 100℃(沸点)に達するまでの顕熱(飽和水のエンタルピーh‘)、飽和水が全て蒸気になったときの全熱量(飽和蒸気のエンタルピーh”)、そしてその蒸発に必要な潜熱(蒸発のエンタルピーr=h”-h’)が、各々示されています。飽和水が蒸発しつつある状態での蒸気は水と共存しているため湿り飽和蒸気と呼び、全て蒸発しきった状態の蒸気を乾き飽和蒸気と呼んでいます。乾き飽和蒸気をさらに加熱すると、再び温度が上昇していきます。この飽和温度よりも高い温度の蒸気を過熱蒸気と呼び、その過熱蒸気と飽和蒸気の温度差を過熱度と呼んでいます。
以後、水のエンタルピーを"顕熱"、蒸発のエンタルピーを"潜熱"、蒸気の保有する熱を"全熱"と表記します。
-
蒸気のエネルギー
これまで述べたことから明らかなように、蒸気は、加熱等に使用されてその潜熱を失った後は相変化して復水になりますが、その時点の温度は蒸気と同じです。この特性を持つ潜熱は、一定温度で安定した加熱処理を必要とするプロセスや殺菌等において極めて有効なエネルギーとなります。蒸気がエネルギーの運び手として優れている理由は、非常に大きな潜熱を保有できる、ありふれた物質だからです。
この潜熱の大きさは飽和蒸気表で簡単に確認できます。表 1.2 は飽和蒸気表のデータを一部抜粋したものです。例えば、大気圧(ゲージ圧 0.0MPa)では、次の値が記載されています(小数点以下1位を四捨五入しています)。
飽和水の顕熱 h’=419 kJ/kg
蒸気の全熱 h”=2,676 kJ/kg
潜熱 r=h”-h’=2,257 kJ/kg従って、
(蒸気の全熱に対する潜熱の割合) =2,257/2,676=0.8434≒84%
(蒸気が保有する潜熱の顕熱に対する大きさ) =2,257/419=5.3866≒5.39
このように、大気圧下の蒸気は、その全熱のうち 84%が潜熱であり、顕熱の
5.39 倍も大きな値であることが分かります。
表 1.1 に、比較的身近に存在する物質である水、アンモニア、メタノール、エタノールの熱物性を掲載しています。相対的に水の蒸発熱が著しく大きいことが分かります。
表 1.1 大気圧下における主要物質の熱物性
物質
融点(℃)
沸点(℃)
融解熱(kJ/kg)
蒸発熱(kJ/kg)
水
0
100
333.5
2,257
アンモニア
-77.8
-33.4
338
1,371
メタノール
-97.7
64.7
99.2
1,190
エタノール
-114.1
78.6
109
855
圧力が上昇すると、飽和に至るまでにはさらに熱量が必要で、温度も相変化なく上昇します。即ち、顕熱と飽和温度の両方が増加します。この関係を示すものが、図 1.2 の蒸気飽和曲線です。この曲線上では、水も蒸気も同じ飽和温度で共存し得ます。曲線より下は未だ飽和温度に至っていない水であり、曲線より上は過熱蒸気です。
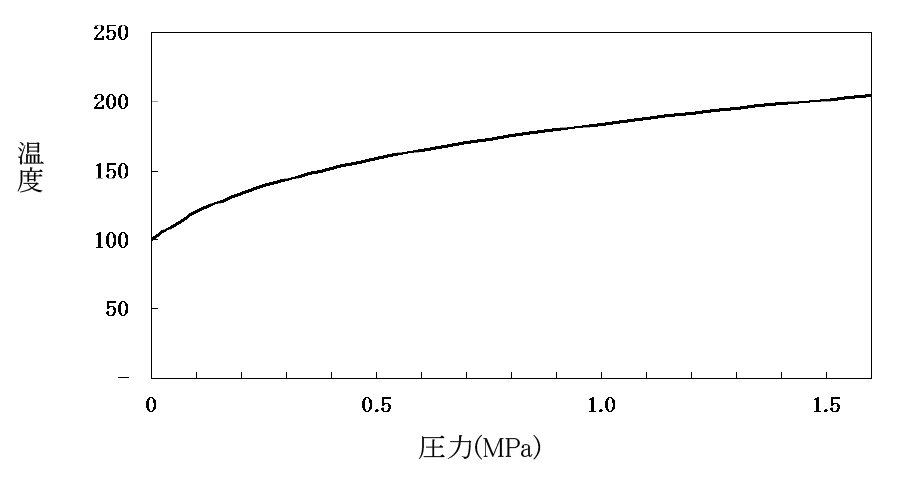
図 1.2 蒸気飽和曲線
では、蒸気や飽和水の熱量は、圧力の上昇と共にどうなるのでしょうか?図 1.3がその関係を示すグラフです。この図から、次のことが簡単に読み取れます。
①飽和水の顕熱は圧力上昇と共に増加する(上述した通り)。
②蒸気の潜熱は圧力上昇と共に減少する。
③蒸気の全熱(上記①の顕熱と②の潜熱の和)は圧力上昇に対して、低圧域では少し増加するものの、ほぼ一定である。(しかしながら、圧力 3.2MPa 付近からは逆に減少し、臨界点に至っては潜熱が零となります。)
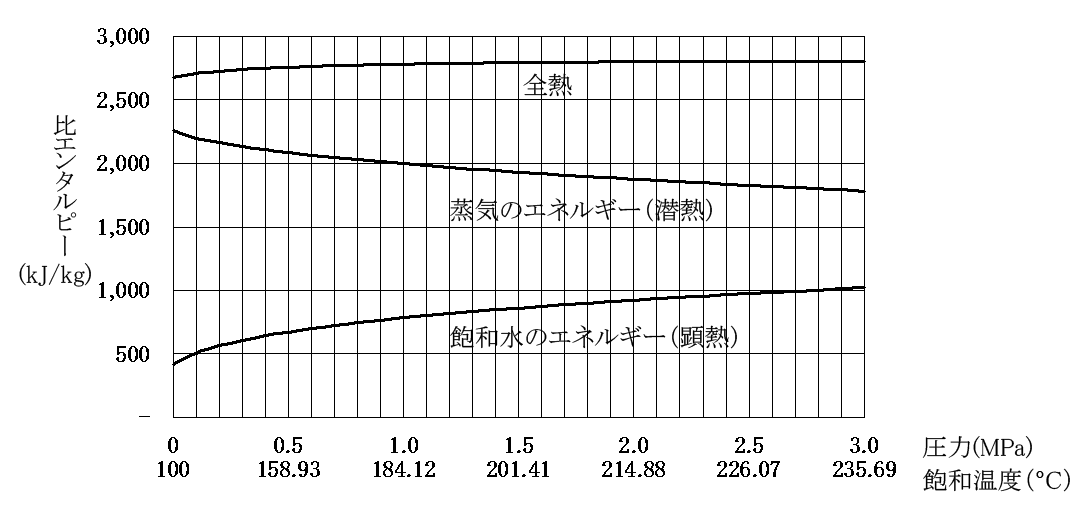
図 1.3 蒸気及び飽和水の熱量と圧力の関係
ここで注意すべきことは、圧力の上昇に伴い、蒸発に必要な潜熱が減少することです。これは、圧力の高い蒸気ほど利用できる潜熱が少ないこと意味します。例えば、表 1.2 の飽和蒸気表より、圧力 0.5MPa と 1.0MPa の潜熱 r は、各々 2,085kJ/kg、1,998kJ/kg と、1.0MPa の方が小さく、また何れも大気圧 0.0MPaでの 2,257kJ/kg より小さな値になっています。
次に、蒸気の比容積と圧力の関係を図 1.4 で見てみます。図から明らかなように、比容積は低圧域では大きく変化し、高圧になるにつれて小さくなる反比例的な変化を示します。圧力が高いほど単位質量(1kg)当たりの潜熱は減少しますが、その容積も減少し、結果として単位容積(1m3)当たりの潜熱は増加します。従って、蒸気圧力を高くすることにより、相対的に小さなサイズの蒸気輸送管でより多くのエネルギーを運ぶことが可能です。このことは蒸気配管系の設計に際して考慮されるべき重要ポイントの1つです。
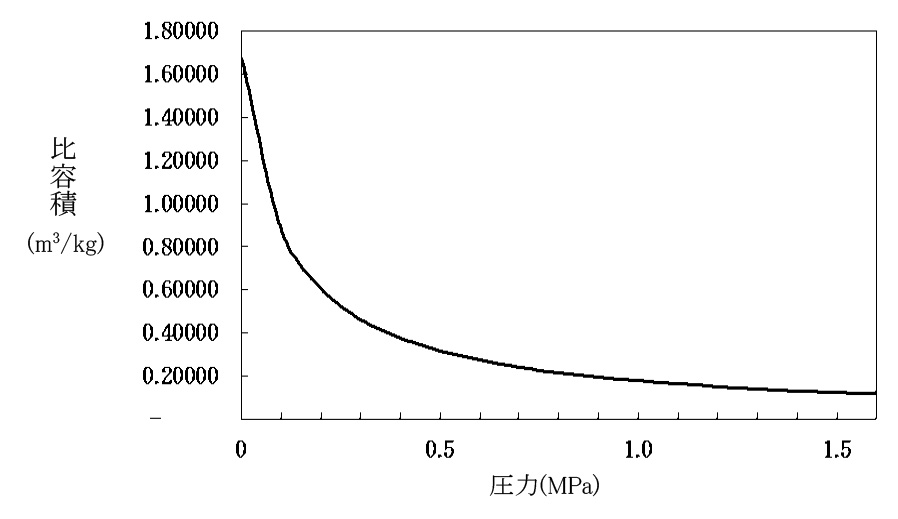
図 1.4 蒸気圧力と比容積の関係
表 1.2 飽和蒸気表(ゲージ圧力基準)
ゲージ圧力(MPa)
飽和温度(℃)
比容積 (m3/kg)
比重量 (kg/m3)
蒸発熱(kJ/kg)
飽和水
飽和蒸気
顕熱
全熱
潜熱
v’
v”
h’
h”
r=h”-h’
0.0
100.00
0.0010437
1.67300
0.5977
419.06
2676.0
2256.9
0.1
120.44
0.0010610
0.87999
1.1364
505.58
2706.6
2201.0
0.5
158.93
0.0011096
0.31482
3.1764
670.79
2755.6
2084.7
1.0
184.12
0.0011331
0.17718
5.6440
781.36
2779.7
1998.3
-
乾き度
蒸気はボイラで生成されて各使用場所へ輸送されますが、ボイラで水分を全く含まない蒸気を生成することは、まず不可能に近く、不可避的に多少の水分を含んでしまいます。しかしながら、蒸気を使用する側からすれば、水分を全く含まない乾き飽和蒸気が望まれます。この水分含有量の少なさを乾き度(Dryness fraction)と呼んでおり、乾き度が高いほど‘蒸気の質
(Quality)’が良いと言います。
乾き度(χ)は、蒸気の重量に対する渇き蒸気の重量比率です。例えば、蒸気が 5%の水分を含んでいる場合の乾き度は、0.95 です。因みに(1-χ)を湿り度と呼んでいます。ボイラ出口の蒸気の乾き度は、概ね 0.95~0.98 で す。湿り飽和蒸気の持つ熱量(比エンタルピー h)は、図 1.1 の記号を用いると次式で表されます。
h=(1-χ)h’+χh”=h’+χr
-
フラッシュ蒸気
フラッシュ蒸気(Flash steam)という言葉は、一般的に、復水レシーバのベントやスチームトラップ二次側の開放復水配管から生じる蒸気を表現するために使われています。熱を加えないのにどうして蒸気が生成されるのでしょうか?フラッシュ蒸気は、ある圧力の水がそれより低い圧力に晒されるとき、その水の温度がその低い圧力の飽和温度より高い場合に必ず発生します。
例として、復水がスチームトラップを通過する場合を考えます。このようなケースでは、一次側の温度は、フラッシュ蒸気を発生させるのに十分高い場合が殆どです。
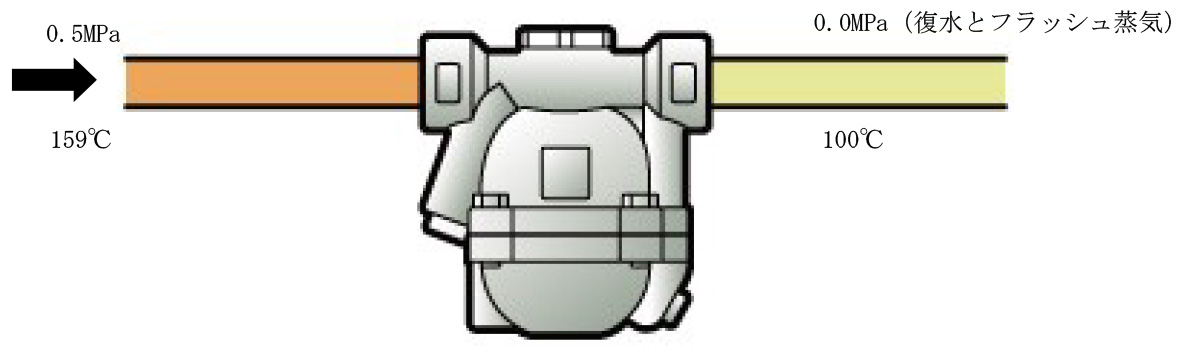
図 1.5 フラッシュ蒸気の生成
図 1.5 において、スチームトラップ一次側の圧力が 0.5MPa で、その飽和温度 159℃の復水 1kg が、大気開放(0.0MPa)の復水配管へ排出されています。
表 1.2 より、0.5MPa の飽和温度の復水 1kg が保有する顕熱は 671kJ です。熱力学の第 1 法則より、流体の全熱量はスチームトラップの高圧側と低圧側で等しく、これは一般にエネルギー保存則に従うものです(スチームトラップ内での放熱や流路抵抗による熱損失は無視しています)。従って、低圧側へ流れた水 1kg も 671kJの熱を保有することになります。しかし、圧力 0.0MPa 下での水は 419kJ の熱しか保有できず、671-419=252kJ の熱の不均衡が生じてしまいます。これは、水の側から見れば余剰熱となりますが、この余剰熱が復水の一部を沸騰させて、いわゆるフラッシュ蒸気を生成させます。
従って、トラップの高圧側では液体として存在していた復水 1kg は、低圧側では、液体と一部蒸気の形で存在することになります。
生成されるフラッシュ蒸気量は、次式を用いて計算できます。

従って、復水 1kg 当りのフラッシュ蒸気生成量は 0.11kg となります。
フラッシュ蒸気の生成割合は、その最終圧力における余剰熱と潜熱の割合と考えることができます。
重要なことは、フラッシュ蒸気は単に蒸気システム内やその終端出口で自然発生的に生じる現象としてとらえるのではなく、蒸気の有効活用のために積極的に利用すべきものだということです。フラッシュ蒸気を利用するための代表的な機器として、フラッシュタンクがあります。
-
その他の特性
蒸気がエネルギーの運び手として広く利用されている主な理由として、保有潜熱が大きいこと、水が地球上に多量に存在して経済的であること等は既に述べた通りですが、その他にも次の点を挙げることができます。
- 人体に無害である。
- 腐食性に乏しく、また引火の危険性が無い等、化学的に安定している。
- 他の加熱媒体に比べ、均一な加熱を行うことに優れている。
- 圧力を変えることで温度が変えられるため、要求温度に応じて供給ができる。
- 蒸気と復水の比容積の差が大きいため、蒸気が凝縮するとすぐに新たな蒸気が供給される。
蒸気使用の課題事項としては、次の点が挙げられます。
- ボイラでの蒸気生成過程やその後のプロセスで空気等の混入を完全防止することができず、その混入空気によって伝熱効率が低下する。
- 蒸気を生成する原水は純水ではないために酸化腐食の原因となる不純物が溶存しており、蒸気生成過程でそれらを完全除去できない。
-
スチームトラップにとっては、水の凝固点が 0℃であるため、地域によっては凍結防止対策を要することも挙げられます。